×
Login Form
×
Registrierung
Profile Informationen
Login Daten
oder Einloggen
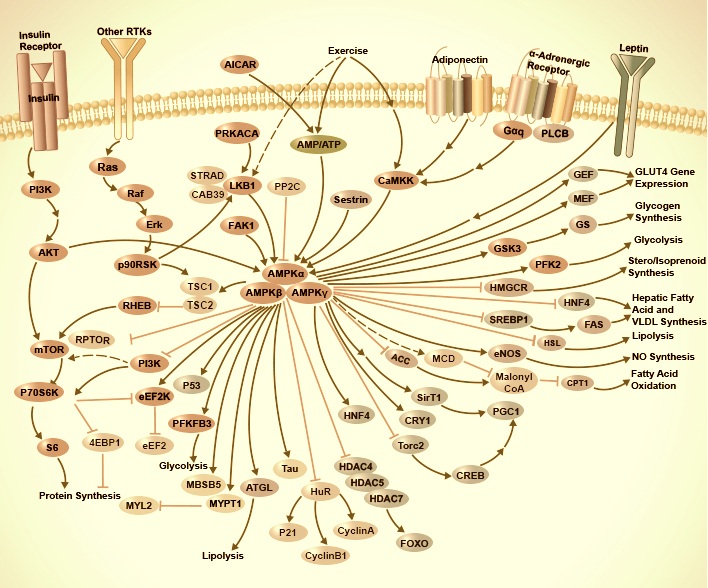
AMPK Signalweg
Der AMPK-Signalweg, ein Treibstoffsensor und -regler, fördert die ATP-Produktion und hemmt die ATP-verbrauchenden Stoffwechselwege in verschiedenen Geweben. AMPK existiert als heterotrimerer Komplex, der aus einer katalytischen α-Untereinheit und einer regulatorischen β- und γ-Untereinheiten besteht. Die Kinase wird als Reaktion auf Belastungen aktiviert, die zelluläre ATP-Zufuhren wie niedrige Glukose, Hypoxie, Ischämie und Hitzeschock depletieren. Die Bindung von AMP an die γ-Untereinheit aktiviert allosterisch den Komplex und macht ihn zu einem attraktiveren Substrat für seine hauptsächliche AMPK-Kinase, LKB1. Als zellulärer Energiesensor, der auf niedrige ATP-Spiegel reagiert, reguliert die AMPK-Aktivierung Signalwege, die zelluläre ATP-Versorgungen auffüllen. Zum Beispiel steigert die Aktivierung von AMPK sowohl die Transkription als auch die Translokation von GLUT4, was zu einer Erhöhung der Insulin-stimulierten Glukoseaufnahme führt. Darüber hinaus stimuliert es katabole Prozesse wie Fettsäureoxidation und Glykolyse durch Hemmung von ACC und Aktivierung von PFK2. AMPK reguliert mehrere Proteine, die für ATP-konsumierende Prozesse, wie TORC2, die Glykogensynthase, SREBP-1 und TSC2 zentral sind, negativ, was zu einer Herabregulierung oder Hemmung der Glukoneogenese, Glykogen-, Lipid- und Proteinsynthese führt. Aufgrund seiner Rolle als zentraler Regulator sowohl des Lipid- als auch des Glukosestoffwechsels wird AMPK als ein therapeutisches Schlüsselziel für die Behandlung von Fettleibigkeit, Typ-II-Diabetes mellitus und Krebs angesehen. Die AMP-aktivierte Proteinkinase (AMPK) spielt eine wichtige Rolle bei der Regulation der zellulären Energiehomöostase. Das Enzym wird durch niedrige ATP Bedingungen aktiviert, was oft durch eine Vielzahl von Stressfaktoren verursacht wird und reguliert Signalwege, die die Verfügbarkeit von ATP erhöhen.
AMPK Signalweg von A bis Z
Thanks to Sino Biological for providing the pathways.