×
Login Form
×
Registrierung
Profile Informationen
Login Daten
oder Einloggen
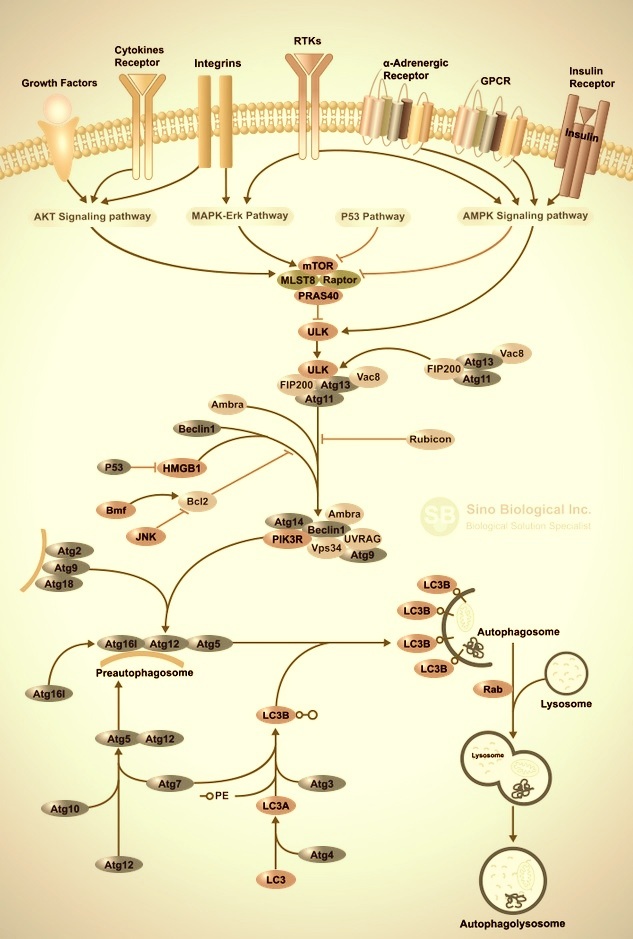
Autophagie-Weg
Autophagie, für die 2016 der Nobelpreis für Physiologie oder Medizin vergeben wurde, ist ein dynamisches Zellrecycling-System, das zum autophagosomalen bzw. lysosomalen Abbau von zytoplasmatischen Inhaltsstoffen, abnormalen Proteinaggregaten und überschüssigen oder beschädigten Organellen führt. Der kritische Regulator der Autophagie-Induktion ist die mTOR-Kinase. Die aktivierte Form (Akt- und MAPK-Signalgebung) unterdrückt die Autophagie und die negative Regulation der mTOR-Kinase (AMPK- und p53-Signalgebung), fördert sie. Die ULK, die eine ähnliche Rolle wie die Hefe Atg1 spielt, wirkt downstream des mTOR-Komplexes. ULK bildet mit Atg13 und dem Gerüstprotein FIP200 einen großen Komplex. Der Klasse-III-PI3K-Komplex, enthaltend hVps34, Beclin-1 (ein Säugetier-Homolog von Hefe Atg6), p150 (ein Säugetier-Homolog von Hefe-Vps15) und Atg14-ähnliches Protein (Atg14L oder Barkor) oder Ultraviolettbestrahlungsresistenz-assoziiertes Gen (UVRAG) , ist für die Induktion der Autophagie erforderlich. Rubicon hemmt die PI3K-Klasse-III-Lipidkinase-Aktivität und wirkt Atg14L entgegen, einem Verstärker der PI3K-Klasse-III-Aktivität. Die Atg-Gene kontrollieren die Autophagosomenbildung durch Atg12-Atg5- und LC3-II (Atg8-II) -Komplexe. Atg12 ist mit Atg5 in einer Ubiquitin-ähnlichen Reaktion konjugiert, die Atg7 und Atg10 benötigt (E1 bzw. E2-artige Enzyme). Das Atg12-Atg5-Konjugat interagiert dann nichtkovalent mit Atg16 unter Bildung eines großen Komplexes. Der zweite Komplex, LC3 / Atg8, wird an seinem C-Terminus durch Atg4-Protease gespalten, um das cytosolische LC3-I zu erzeugen. LC3-I ist an Phosphatidylethanolamin (PE) in einer Ubiquitin-ähnlichen Reaktion konjugiert, die Atg7 und Atg3 benötigt (E1 bzw. E2-artige Enzyme). Die lipidierte Form von LC3, bekannt als LC3-II, ist an die Autophagosom-Membran gebunden. Autophagie und Apoptose sind sowohl positiv als auch negativ miteinander verbunden, und es besteht ein weitgehendes Übersprechen zwischen den beiden Prozessen. Während eines Nährstoffmangels fungiert die Autophagie als pro-Überlebensmechanismus; Übermäßige Autophagie kann jedoch zum Zelltod führen, ein Prozess, der sich morphologisch von der Apoptose unterscheidet. Mehrere pro-apoptotische Signale, wie TNF, TRAIL und FADD, induzieren ebenfalls Autophagie. Zusätzlich inhibiert Bcl-2 die Beclin-1-abhängige Autophagie, wodurch es sowohl als Pro-Überlebens- als auch als Antiautophage-Regulator fungiert.
Autophagie Weg von A bis Z
Vielen Dank an Sino Biological für die Bereitstellung der Signalwege.